Кахексията е системно заболяване, характеризиращо се със загуба на тегло, атрофия на мускулната и мастната тъкан и системно възпаление. Кахексията е едно от основните усложнения и причини за смърт при онкоболни. Смята се, че честотата на кахексията при онкоболни може да достигне от 25% до 70%, а около 9 милиона души по света страдат от кахексия всяка година, като се очаква 80% от тях да починат в рамките на една година след поставяне на диагнозата. Освен това, кахексията значително влияе върху качеството на живот на пациентите и изостря токсичността, свързана с лечението.
Ефективната интервенция при кахексия е от голямо значение за подобряване на качеството на живот и прогнозата на онкологичните пациенти. Въпреки известния напредък в изучаването на патофизиологичните механизми на кахексията, много лекарства, разработени въз основа на възможни механизми, са само частично ефективни или неефективни. Понастоящем няма ефективно лечение, одобрено от Американската агенция по храните и лекарствата (FDA).
Кахексията (синдром на изтощение) е много често срещана при пациенти с много видове рак, което често води до загуба на тегло, мускулна атрофия, намалено качество на живот, нарушена функция и съкратена преживяемост. Според международно приетите стандарти, този многофакторен синдром се определя като индекс на телесна маса (ИТМ, тегло [kg], разделено на височина [m] на квадрат) по-малък от 20 или, при пациенти със саркопения, загуба на тегло с повече от 5% за шест месеца или загуба на тегло с повече от 2%. Понастоящем в Съединените щати и Европа не са одобрени лекарства специално за лечение на ракова кахексия, което води до ограничени възможности за лечение.
Последните насоки, препоръчващи ниски дози оланзапин за подобряване на апетита и теглото при пациенти с напреднал рак, се основават до голяма степен на резултатите от едноцентрово проучване. В допълнение към това, краткосрочната употреба на прогестеронови аналози или глюкокортикоиди може да донесе ограничени ползи, но съществува риск от нежелани странични ефекти (като употребата на прогестерон, свързана с тромбоемболични събития). Клиничните изпитвания на други лекарства не са успели да покажат достатъчна ефикасност, за да получат регулаторно одобрение. Въпреки че анаморин (перорална версия на пептиди, освобождаващи растежен хормон) е одобрен в Япония за лечение на ракова кахексия, лекарството само до известна степен е увеличило телесния състав, не е подобрило силата на захвата и в крайна сметка не е одобрено от Американската агенция по храните и лекарствата (FDA). Съществува спешна нужда от безопасни, ефективни и целенасочени лечения за ракова кахексия.
Факторът на растежна диференциация 15 (GDF-15) е стрес-индуциран цитокин, който се свързва с глиално-производния невротрофичен фактор, рецепторен алфа-подобен протеин (GFRAL) в задната част на мозъка. GDF-15-GFRAL пътят е идентифициран като основен регулатор на анорексията и регулирането на теглото и играе роля в патогенезата на кахексията. В животински модели GDF-15 може да индуцира кахексия, а инхибирането на GDF-15 може да облекчи този симптом. Освен това, повишените нива на GDF-15 при пациенти с рак са свързани с намалено телесно тегло и маса на скелетните мускули, намалена сила и съкратена преживяемост, което подчертава стойността на GDF-15 като потенциална терапевтична цел.
Понсегромаб (PF-06946860) е високоселективно хуманизирано моноклонално антитяло, способно да се свързва с циркулиращия GDF-15, като по този начин инхибира взаимодействието му с GFRAL рецептора. В малко отворено проучване фаза 1b, 10 пациенти с ракова кахексия и повишени нива на циркулиращия GDF-15 са лекувани с понсегромаб и показват подобрения в теглото, апетита и физическата активност, докато серумните нива на GDF-15 са инхибирани и нежеланите реакции са ниски. Въз основа на това проведохме клинично проучване фаза 2, за да оценим безопасността и ефикасността на понсегромаб при пациенти с ракова кахексия с повишени нива на циркулиращия GDF-15, в сравнение с плацебо, за да тестваме хипотезата, че GDF-15 е основната патогенеза на заболяването.
Проучването включва възрастни пациенти с кахексия, свързана с рак (недребноклетъчен рак на белия дроб, рак на панкреаса или колоректален рак) със серумно ниво на GDF-15 най-малко 1500 pg/ml, оценка за фитнес статус по скалата на Eastern Tumor Consortium (ECOG) ≤3 и продължителност на живота най-малко 4 месеца.
Включените пациенти бяха разпределени на случаен принцип да получават 3 дози понсегромаб 100 mg, 200 mg или 400 mg, или плацебо, подкожно на всеки 4 седмици в съотношение 1:1:1. Първичната крайна точка беше промяната в телесното тегло спрямо изходното ниво на 12-та седмица. Ключовата вторична крайна точка беше промяната от изходното ниво в скалата за анорексия кахексия (FAACT-ACS), оценка на терапевтичната функция за анорексия кахексия. Други вторични крайни точки включваха дневникови резултати за симптомите на кахексия, свързана с рак, изходни промени във физическата активност и крайни точки за походка, измерени с помощта на носими цифрови здравни устройства. Минималните изисквания за време на носене са предварително определени. Оценката на безопасността включваше броя на нежеланите събития по време на лечението, резултатите от лабораторните изследвания, жизнените показатели и електрокардиограмите. Експлораторните крайни точки включваха изходни промени в индекса на лумбалните скелетни мускули (площта на скелетните мускули, разделена на квадрата на височината), свързан със системните скелетни мускули.
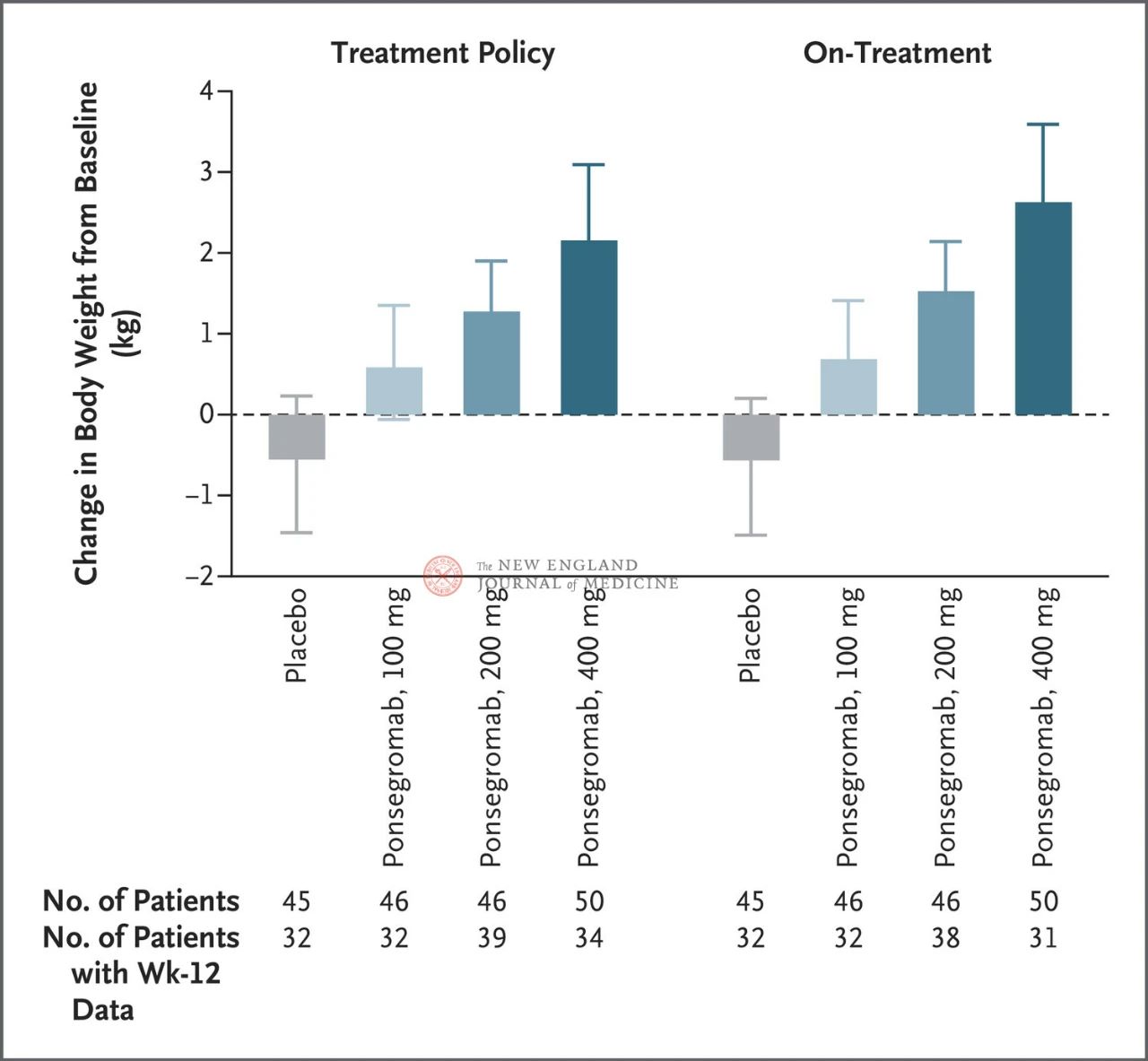
Общо 187 пациенти са били разпределени на случаен принцип да получават понсегромаб 100 mg (46 пациенти), 200 mg (46 пациенти), 400 mg (50 пациенти) или плацебо (45 пациенти). Седемдесет и четири (40%) са имали недребноклетъчен рак на белия дроб, 59 (32%) са имали рак на панкреаса и 54 (29%) са имали колоректален рак.
Разликите между групите със 100 mg, 200 mg и 400 mg и плацебо са съответно 1,22 kg, 1,92 kg и 2,81 kg.
Фигурата показва първичната крайна точка (промяна в телесното тегло от изходното ниво до 12 седмици) при пациенти с ракова кахексия в групите с понсегромаб и плацебо. След коригиране за конкуриращия се риск от смърт и други едновременни събития, като например прекъсване на лечението, първичната крайна точка е анализирана чрез стратифициран Emax модел, използвайки резултати от 12-та седмица от Bayesov съвместен лонгитудинален анализ (вляво). Първичните крайни точки също са анализирани по подобен начин, като са използвани очаквани цели за действителното лечение, където наблюденията след всички едновременни събития са съкратени (дясна фигура). Доверителни интервали (посочени в статията
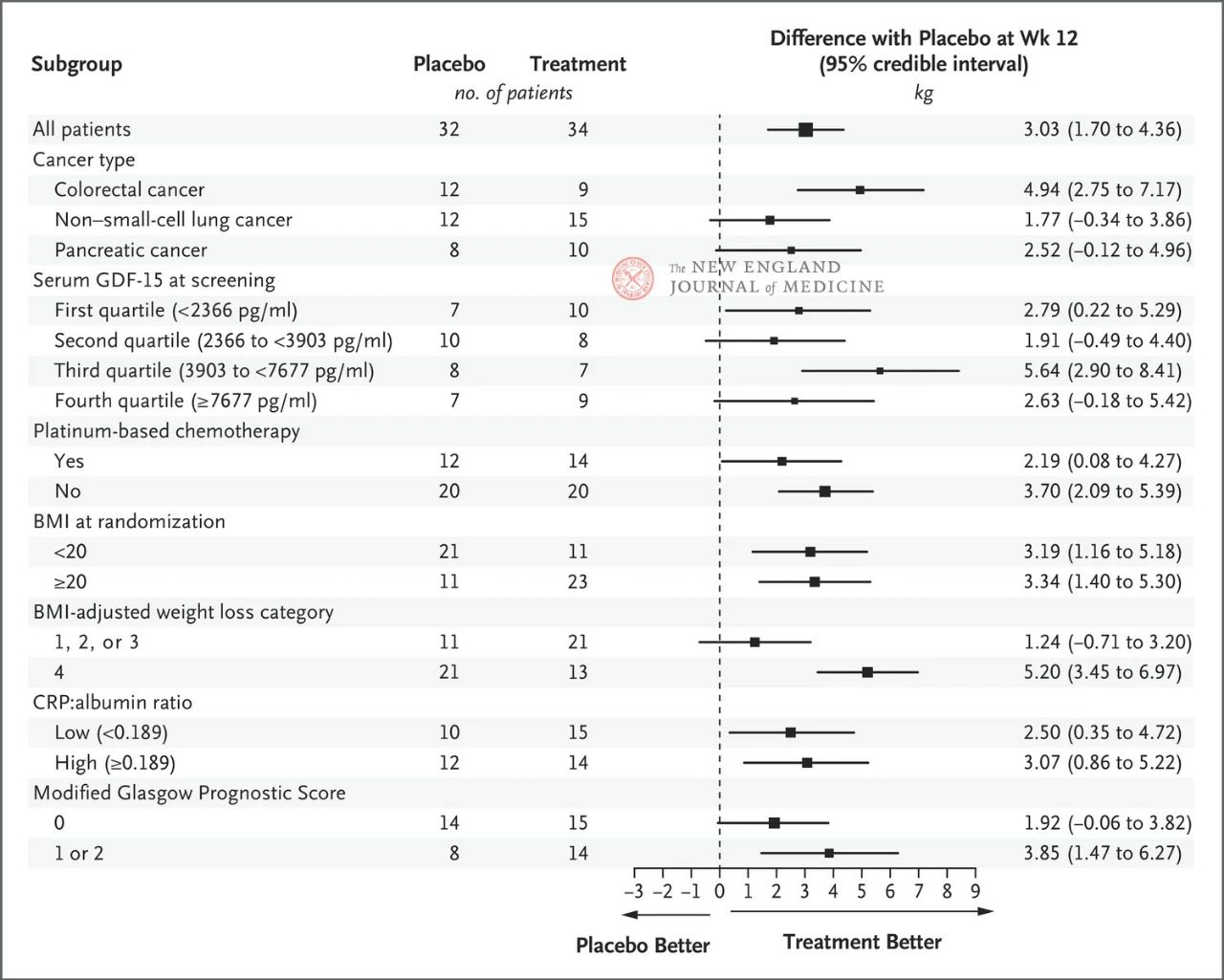
Ефектът на 400 mg понсегромаб върху телесното тегло е бил последователен в основните предварително дефинирани подгрупи, включително вид рак, квартил на серумното ниво на GDF-15, експозиция на химиотерапия на базата на платина, ИТМ и системно възпаление на изходно ниво. Промяната в теглото е била съвместима с инхибирането на GDF-15 на 12-та седмица.
Изборът на ключови подгрупи се основаваше на post-hoc Bayesov съвместен лонгитудинален анализ, проведен след корекция за конкурентния риск от смърт въз основа на очакваната цел на лечебната стратегия. Доверителните интервали не трябва да се използват като заместител на тестването на хипотези без множество корекции. ИТМ представлява индекс на телесна маса, CRP представлява C-реактивен протеин, а GDF-15 представлява фактор на растежна диференциация 15.
В началото на изследването, по-висок процент пациенти в групата, приемаща понсегромаб 200 mg, не съобщават за намаление на апетита; в сравнение с плацебо, пациентите в групите, приемащи понсегромаб 100 mg и 400 mg, съобщават за подобрение на апетита спрямо изходното ниво на 12-та седмица, с повишаване на FAACT-ACS резултатите съответно от 4,12 и 4,5077. Няма значителна разлика в FAACT-ACS резултатите между групата, приемаща 200 mg, и групата, приемаща плацебо.
Поради предварително определени изисквания за време на носене и проблеми с устройството, съответно 59 и 68 пациенти предоставиха данни за промените във физическата активност и крайните точки на походката спрямо изходното ниво. Сред тези пациенти, в сравнение с групата на плацебо, пациентите в групата с 400 mg показаха повишение на общата активност на 12-та седмица, с увеличение от 72 минути не-заседнала физическа активност на ден. Освен това, групата с 400 mg също показа повишение на индекса на лумбалните скелетни мускули на 12-та седмица.
Честотата на нежеланите реакции е била 70% в групата на понсегромаб, в сравнение с 80% в групата на плацебо, и са се наблюдавали при 90% от пациентите, получаващи едновременно системна противоракова терапия. Честотата на гадене и повръщане е била по-ниска в групата на понсегромаб.
Време на публикуване: 05 октомври 2024 г.