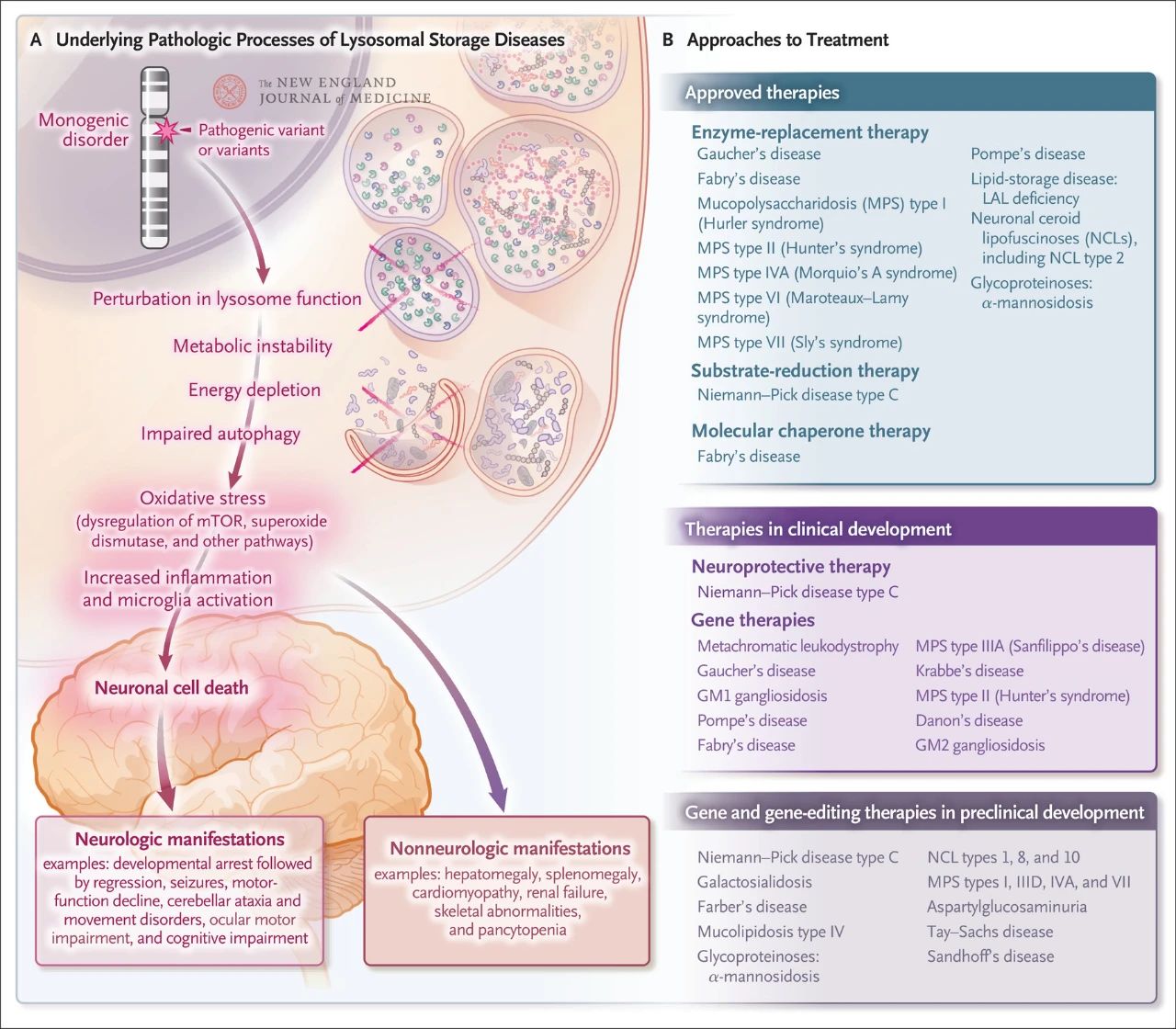
Въпреки че е сравнително рядко, общата честота на лизозомно натрупване е около 1 на всеки 5000 живородени деца. Освен това, от близо 70-те известни лизозомни нарушения на натрупването, 70% засягат централната нервна система. Тези нарушения, свързани с един ген, причиняват лизозомна дисфункция, което води до метаболитна нестабилност, нарушена регулация на рапамицин, целеви протеин при бозайниците (mTOR, който обикновено инхибира възпалението), нарушена автофагия и смърт на нервните клетки. Няколко терапии, насочени към основните патологични механизми на лизозомното натрупване, са одобрени или са в процес на разработка, включително ензимно-заместителна терапия, терапия за намаляване на субстрата, молекулярна шаперонова терапия, генна терапия, генно редактиране и невропротективна терапия.
Болестта на Ниман-Пик тип C е нарушение на клетъчния транспорт на холестерол в лизозомите, причинено от биалелни мутации в NPC1 (95%) или NPC2 (5%). Симптомите на болестта на Ниман-Пик тип C включват бърз, фатален неврологичен упадък в ранна детска възраст, докато късните ювенилни, ювенилни и възрастни форми включват спленомегалия, супрануклеарна парализа на погледа и церебеларна атаксия, дизартикулация и прогресивна деменция.
В този брой на списанието, Бремова-Ертл и др. съобщават за резултатите от двойносляпо, плацебо-контролирано, кръстосано проучване. В проучването е използван потенциален невропротективен агент, аминокиселинният аналог N-ацетил-L-левцин (NALL), за лечение на болестта на Ниман-Пик тип C. В проучването са включени 60 симптоматични юноши и възрастни пациенти и резултатите показват значително подобрение в общия резултат (първична крайна точка) по скалата за оценка и оценка на атаксията.
Клиничните изпитвания на N-ацетил-DL-левцин (Танганил), рацемичен продукт на NALL и n-ацетил-D-левцин, изглежда до голяма степен се обуславят от опита: механизмът на действие не е ясно изяснен. N-ацетил-DL-левцин е одобрен за лечение на остър световъртеж от 50-те години на миналия век; животински модели показват, че лекарството действа чрез ребалансиране на свръхполяризацията и деполяризацията на медиалните вестибуларни неврони. Впоследствие Strupp et al. съобщават за резултатите от краткосрочно проучване, в което наблюдават подобрения в симптомите при 13 пациенти с дегенеративна церебеларна атаксия с различна етиология, открития, които възобновяват интереса към лекарството.
Механизмът, чрез който n-ацетил-DL-левцинът подобрява нервната функция, все още не е ясен, но откритията в два миши модела, единият с болестта на Ниман-Пик тип C, а другият с GM2 ганглиозидно разстройство на съхранението на вариант O (болест на Сандхоф), друго невродегенеративно лизозомно заболяване, накараха вниманието да се насочи към NALL. По-конкретно, преживяемостта на Npc1-/- мишки, третирани с n-ацетил-DL-левцин или NALL (L-енантиомери), се подобри, докато преживяемостта на мишки, третирани с n-ацетил-D-левцин (D-енантиомери), не се подобри, което предполага, че NALL е активната форма на лекарството. В подобно проучване на GM2 ганглиозидно разстройство на съхранението на вариант O (Hexb-/-), n-ацетил-DL-левцинът доведе до умерено, но значително удължаване на живота на мишките.
За да изследват механизма на действие на n-ацетил-DL-левцин, изследователите изследвали метаболитния път на левцина чрез измерване на метаболитите в церебеларните тъкани на мутиралите животни. В вариант О модел на разстройство на съхранението на GM2 ганглиозиди, n-ацетил-DL-левцин нормализира метаболизма на глюкозата и глутамата, увеличава автофагията и повишава нивата на супероксид дисмутаза (активен уловител на кислород). В C модела на болестта на Нийман-Пик са наблюдавани промени в метаболизма на глюкозата и антиоксидантите и подобрения в енергийния метаболизъм на митохондриите. Въпреки че L-левцинът е мощен mTOR активатор, не е наблюдавана промяна в нивото или фосфорилирането на mTOR след лечение с n-ацетил-DL-левцин или неговите енантиомери в нито един от миши модели.
Невропротективният ефект на NALL е наблюдаван в миши модел на мозъчно увреждане, предизвикано от кортикален импингмент. Тези ефекти включват понижаване на невровъзпалителните маркери, намаляване на смъртта на кортикалните клетки и подобряване на автофагичния поток. След лечение с NALL, двигателните и когнитивните функции на увредените мишки са възстановени, а размерът на лезията е намален.
Възпалителният отговор на централната нервна система е отличителен белег на повечето невродегенеративни лизозомни нарушения на съхранение. Ако невровъзпалението може да бъде намалено с лечение с NALL, клиничните симптоми на много, ако не и на всички, невродегенеративни лизозомни нарушения на съхранение могат да бъдат подобрени. Както показва това проучване, се очаква NALL да има синергия с други терапии за лизозомни заболявания на съхранение.
Много лизозомни нарушения на съхранението също са свързани с церебеларна атаксия. Според международно проучване, включващо деца и възрастни с нарушения на съхранението на GM2 ганглиозиди (болест на Тей-Сакс и болест на Сандхоф), атаксията е намалена и фината двигателна координация се е подобрила след лечение с NALL. Въпреки това, голямо, многоцентрово, двойносляпо, рандомизирано, плацебо-контролирано проучване показва, че n-ацетил-DL-левцин не е клинично ефективен при пациенти със смесена (наследствена, ненаследствена и необяснима) церебеларна атаксия. Това откритие предполага, че ефикасността може да се наблюдава само в проучвания, включващи пациенти с наследствена церебеларна атаксия и анализирани свързаните с нея механизми на действие. Освен това, тъй като NALL намалява невровъзпалението, което може да доведе до травматично мозъчно увреждане, могат да се обмислят проучвания на NALL за лечение на травматично мозъчно увреждане.
Време на публикуване: 02 март 2024 г.